ალდეჰიდის საწყობი რომ ბუდოვა. ალდეჰიდების და კეტონების ფიზიკური და ქიმიური ძალა. ნომენკლატურა და იზომერია
ავტორიტეტების პირველი ჯგუფი არის მარხვის რეაქციები. კარბონილის ჯგუფში, ქვანახშირსა და მაწონს შორის, არის ძირითადი ბმული, რომელიც, როგორც გახსოვთ, წარმოიქმნება სიგმა-ბმულისა და p-ბმულისგან. რეაქციებში პი-ბმულების ჩამოსვლა წყდება და იქმნება ორი სიგმა ბმული - ერთი ნახშირით, მეორე მაწონით. ნახშირზე არის ნაწილობრივი დადებითი მუხტი, მჟავაზე - ნაწილობრივი უარყოფითი მუხტი. ამასთან, რეაგენტის ნაწილი, ანიონი, უარყოფითად არის დამუხტული ნახშირბადზე, ხოლო მოლეკულის ნაწილი დადებითად დატვირთულია მჟავეზე.
პერჩეელექტროენერგია - წყალმომარაგება, წყალმომარაგება.
რეაქცია ხდება გაცხელების დროს. Zastosovuєtsya vzhe vіdomy katalіzator gidrovannya - ნიკელი. ალდეჰიდებში შედის პირველადი სპირტები, კეტონები მეორადი.
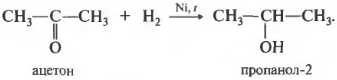
მეორად სპირტებში ჰიდროქსოჯგუფი შეკრულია მეორადი ნახშირბადის ატომისგან.
მეგობარიძალა - დატენიანება, წყლის გამოჩენა. ეს რეაქცია შესაძლებელია მხოლოდ ფორმალდეჰიდისთვის და აცეტალდეჰიდისთვის. კეტონებს მოუწოდებენ არ რეაგირებენ წყალთან.
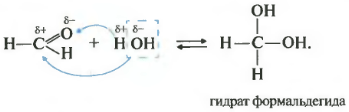
ყველა რეაქცია მოდის ისე, რომ პლუსი მიდის მინუსზე და პლუს მინუსზე.
როგორც გახსოვთ ალკოჰოლების შესახებ ვიდეოდან, ერთ ატომში ორი ჰიდროქსოჯგუფის არსებობა შეიძლება შეუძლებელი იყოს, ამიტომ გამოსვლები ძალიან არათანმიმდევრულია. ასე რომ, დეპრესიის იგივე ორი ციკლის ღერძი - ფორმალდეჰიდის ჰიდრატი და ოქტოური ალდეჰიდი - შეიძლება იყოს, თუ გნებავთ და გამოიყენოთ მხოლოდ საცალო ვაჭრობაში.
თავადაზნაურების რეაქცია ნეობოვიაზკოვოა. ყველაფერზე უკეთესია, სიზმარში კვება შეიძლება ფაქტობრივად ჟღერდეს, ვთქვათ, წყალთან ერთად, მეტყველების პერახოვანია რომ რეაგირებს. მის შუაში შეგიძლიათ გამოიყენოთ მეტანი ჩი ეტანალი.
მესამეძალა - ჰიდროციანმჟავას გამოჩენა.

Znovu plus გადასვლა მინუსზე და მინუს პლუსზე. არის გამოსვლები, რომლებსაც ჰიდროქსიტრილებს უწოდებენ. კარგად ვიცი, თავად რეაქცია იშვიათად ისმის, მაგრამ ძალაუფლების ცოდნა აუცილებელია.
მეოთხედიძალა - ალკოჰოლის ჩამოსვლა.
აქ, ისევ და ისევ, არ არის აუცილებელი თანაბარი რეაქციის დამახსოვრება, უბრალოდ აუცილებელია იმის გაგება, რომ ასეთი ურთიერთქმედება შესაძლებელია.

როგორც წესი, რეაქციებში მიიწევს კარბონილის ჯგუფში პლუს მინუსზე და მინუს პლუსზე.
პიატისიმძლავრე - რეაქცია ნატრიუმის ჰიდროსულფიტთან.

და ისევ, რეაქცია დოზიტზე დასაკეცია, ნაკლებად სავარაუდოა, რომ დანებდეთ, მაგრამ ეს არის ალდეჰიდების ერთ-ერთი აკіსნიური რეაქცია, რომ ნატრიუმის ძალა წყდება და ალყაში მოხვდება. თავადაზნაურობის ბრალია, რომ ალდეჰიდები რეაგირებენ ნატრიუმის ჰიდროსულფიტთან, რაც საკმარისი იქნება.
დავასრულოთ რეაქციების პირველი ჯგუფი. კიდევ ერთი ჯგუფი არის პოლიმერიზაციის და პოლიკონდენსაციის რეაქციები.
2. ალდეჰიდების პოლიმერიზაცია და პოლიკონდენსაცია
ჩვენ ვიცით პოლიმერიზაციის შესახებ: პოლიეთილენის, ბუტადიენისა და იზოპრენის რეზინები, პოლივინილ ქლორიდი - უპიროვნო მოლეკულების (მონომერების) გაერთიანების პროდუქტები ერთ დიდ, ერთ პოლიმერულ ზოლში. Tobto, შეიყვანეთ ერთი პროდუქტი. როდესაც პოლიკონდენსაცია ხდება, იგივეა, მაგრამ პოლიმერი ასევე შეიცავს დაბალი მოლეკულური წონის პროდუქტებს, მაგალითად, წყალს. Tobto out ორი პროდუქტი.
ოტჟე, შოსტესიმძლავრე - პოლიმერიზაცია. კეტონები და რეაქციები არ შედის, სიტყვის მნიშვნელობა მხოლოდ ფორმალდეჰიდის პოლიმერიზაციაა.
პი-ბმული წყდება და სუციდური მონომერებით წარმოიქმნება ორი სიგმა ბმა. გასასვლელი პოლიფორმალდეჰიდი, პარაფორმების სათაურები. Nayimovіrnіshe, іspitі-ზე კვება შეიძლება ასე ჟღერდეს: პოლიმერიზაციის რეაქციები შედის მეტყველებაში. შედგენილია გამოსვლების სია, რომელთა შორის შეიძლება იყოს ფორმალდეჰიდი.
სომა სიმძლავრე - პოლიკონდენსაცია. კიდევ ერთხელ: როდესაც პოლიკონდენსაცია, კრემის პოლიმერი, გამოდის უფრო დაბალი მოლეკულური წონა, მაგალითად, წყალი. ფორმალდეჰიდი მონაწილეობს ფენოლთან ასეთ რეაქციაში. სიცხადისთვის ჩვენ ჩამოვწერთ ამ ორის გათანაბრებას ფენოლის მოლეკულებით.
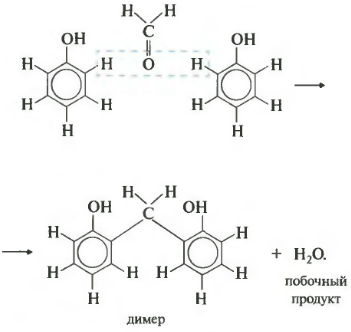
შედეგად, ასეთი დიმერი ჩნდება და წყლის მოლეკულა იშლება. ახლა ჩამოვწეროთ სამარცხვინო მნახველის თანაბარი რეაქცია.

პოლიკონდენსაციის პროდუქტი არის ფენოლ-ფორმალდეჰიდის ფისი. არსებობს აპლიკაციების ფართო სპექტრი - ადჰეზივებისა და ლაქების ტიპები ნაწილაკების დაფების პლასტმასის კომპონენტებზე.
ახლა ძალების მესამე ჯგუფი არის ჟანგვის რეაქციები.
3. ალდეჰიდების და კეტონების დაჟანგვა
მერვერეაქცია პირველ სიაში არის მსგავსი რეაქცია ალდეჰიდის ჯგუფთან - ამონიუმის ოქსიდით დაჟანგვა სრიბლო ოქსიდამდე. ვერცხლის სარკის რეაქცია. კიდევ ერთხელ ვიტყვი, კეტონები არ შედიან ამ რეაქციაში, მხოლოდ ალდეჰიდები.

ალდეჰიდის ჯგუფი იჟანგება კარბოქსილის, მჟავე ჯგუფად, მაგრამ ამიაკის არსებობისას, რომელიც წარმოადგენს ფუძეს, მაშინვე შეინიშნება ნეიტრალიზაციის რეაქცია და გამოიყოფა ამონიუმის აცეტატი. იგი ალყაში ჩავარდა, საცდელი მილი შუაზე გადაატრიალა და სარკის ზედაპირი შექმნა. Tsya რეაქცია zustrichaetsya on ЄDI postіyno.
მეტყველებამდე ეს რეაქცია მჟავეა სხვა მეტყველებაზე, რომელიც შეიძლება შეიცავდეს ალდეჰიდის ჯგუფს, მაგალითად, ჭიანჭველა მჟავას და її მარილებს, ასევე გლუკოზას.
დევიატარეაქცია tezh yakіsna ალდეჰიდის ჯგუფზე - დაჟანგვა ახლად დალექილი ჰიდროქსიდით midi ორი. აქაც პატივს ვცემ, რომ კეტონები არ შედიან ამ რეაქციაში.

ვიზუალურად, შეგიძლიათ ნახოთ ყვითელი ალყის დასაწყისი, რომელიც შემდეგ ხდება ჩერვონიმი. ზოგიერთ ასისტენტში არის ინფორმაცია, რომ ჰიდროქსიდი მიდი მეტ-ნაკლებად დასახლებულია, მას აქვს ყვითელი ფერი, რომელიც შემდეგ იშლება შავ ოქსიდში და წყალში. ასე რომ, ღერძი არასწორია - ალყის დაცემის პროცესში ხარკის დანარჩენი ნაწილისთვის იცვლება მიდის ოქსიდის ნაწილაკების გაფართოება, თითქოს შესაძლებელია გაფართოების მიღწევა, წითელ ფერად გადაქცევა. ალდეჰიდი იჟანგება ორმაგ კარბოქსილის მჟავად. იოგაზე რეაქცია ძალიან ხშირია.
მეათე რეაქცია - ალდეჰიდების დაჟანგვა გაცხელებისას კალიუმის პერმანგანატის მჟავიანობით.
Vіdbuvaєtsya znebarvlennya rozchinu. ალდეჰიდის ჯგუფი იჟანგება კარბოქსილამდე, ისე რომ ალდეჰიდი იჟანგება წყალმჟავად. კეტონებისთვის რეაქციას არ აქვს რაიმე პრაქტიკული აზრი, მაგრამ შეინიშნება მოლეკულის განადგურება და შედეგი არის პროდუქტების ჯამი.
მნიშვნელოვანია აღინიშნოს, რომ ფორმალდეჰიდი, ფორმალდეჰიდი, იჟანგება ნახშირორჟანგამდე, რადგან მურაშინის მჟავა არ არის მდგრადი ძლიერი ოქსიდიზატორების მიმართ.
ომის ნახშირის გასავლელად ჟანგვის სტადიიდან 0 სტადია დაჟანგვა +4. ვხვდები, რომ მეთანოლი, როგორც წესი, ასეთ გონებაში იჟანგება მაქსიმუმ CO 2-მდე, გამოტოვებს სტადიას და ალდეჰიდს და მჟავას. Tsyu sooblivіst slid memorize.
Თერთმეტირეაქცია არის მთა, გარე დაჟანგვა. მე ალდეჰიდები და კეტონები იწვის ნახშირორჟანგს და წყალს.
ჩამოვწეროთ სამარცხვინო მზერის თანაბარი რეაქცია.
კონსერვაციის კანონის მიღმა, ატომების მასები ბოროტია, მაგრამ მათი სტილისტიკა შესაძლებელია, რამდენი ატომია მემარჯვენე. აჯე ქიმიურ რეაქციებში ატომები არსად მიდიან, უბრალოდ ცვლიან მათ შორის ობლიგაციების თანმიმდევრობას. ასე რომ, ნახშირორჟანგის მოლეკულების ღერძი იქნება stilki zh, skіlki і ნახშირბადის ატომები კარბონილის ჯაჭვის მოლეკულებში, ნამსხვრევები მოლეკულის საწყობში მოიცავს ნახშირბადის ერთ ატომს. ასე რომ, არსებობს n CO2 მოლეკულები. წყლის მოლეკულები ორჯერ ნაკლები იქნება, წყლის უფრო დაბალი ატომები, ანუ 2n/2, შემდეგ მხოლოდ n.
Atomіv kisnyu lіvoruch i pravoruch იგივე kіlkіst. მარჯვნივ, їх 2n ნახშირორჟანგიდან, ამიტომ კანის მოლეკულაში არის ორი ჟანგბადის ატომი, პლუს n წყალი, 3n დროს. Livoruch atomіv kisnyu stіlki w - 3n, მაგრამ ერთ-ერთი ატომი გვხვდება ალდეჰიდის მოლეკულაში, რაც იმას ნიშნავს, რომ ის დიდი რიცხვის სახით უნდა ჩაითვალოს, რათა ატომების რიცხვი წაიშალოს, რათა დაეცეს მოლეკულური კისენი. მოლეკულური მჟავის ჩასანაცვლებლად შემოდის 3n-1 ატომები და შესაბამისად 2-ჯერ ნაკლები მოლეკულაა, ამიტომ ერთი მოლეკულის საწყობში 2 ატომი შედის. ტობტო (3n-1)/2 მჟავე მოლეკულა.
ამ რანგში, ველური იერით დავაყარეთ ნახშირბადის ჭურვების ცეცხლი.
მე მაგალითად, თორმეტიძალა, რომელიც მოდის ალფა ნახშირბადის ატომით ჩანაცვლების რეაქციებში - ჰალოგენაცია. კიდევ ერთხელ მივიღებთ ალდეჰიდის მოლეკულას. ოქსიდი ახორციელებს ელექტრონულ მუხტს თავის თავზე, ქმნის ნაწილობრივ დადებით მუხტს ნახშირბადზე. მეთილის ჯგუფი მაგნიტიზებულია დადებითი მუხტის კომპენსაციის მიზნით, გადადის წყალში ახალ ელექტრონზე ლანცეტური სიგმა ვარსკვლავით. ქვანახშირის წყლის ხმა უფრო პოლარული ხდება და წყლის სუნთქვა უფრო ადვილია რეაგენტით შეტევის საათში. ასეთი ეფექტი შესაძლებელია მხოლოდ ნახშირბადის ალფა ატომისთვის, რადგან ატომი, რომელიც მიჰყვება ალდეჰიდის ჯგუფს, დამოუკიდებელია ნახშირწყლების რადიკალისგან.
ამ რანგში შეგიძლიათ წაართვათ, მაგალითად, 2-ქლოროაცეტალდეჰიდი. შესაძლებელია წყალში ატომების ჩანაცვლება ტრიქლორეთანით უფრო შორს.
Oxo ნაერთების კლასამდე არის ორგანული გამოსვლები, რომლებიც შურისძიებას ახდენენ ჯგუფზე >C=O,მე მას კარბონილის ჯგუფს ან კარბონილს ვუწოდებ.
ვინაიდან ნახშირბადის ატომის ორი ვალენტობა დაკავებულია ალკილის რადიკალებით, ოქსო ნახევარსფეროებს კეტონებს უწოდებენ:
ვინაიდან ნახშირბადის ატომისა და კარბონილის ორ ვალენტობას უკავია ალკილის რადიკალები და წყლის ატომები, ოქსო ნახევარსფეროებს ალდეჰიდები ეწოდება.
კეტონებსა და ალდეჰიდებს ასევე უწოდებენ კარბონილის ნაერთებს.
ალდეჰიდების და კეტონების რეაქციები მსგავსია, რაც მათ საშუალებას აძლევს გამოიყურებოდეს ოქსო ნაერთების საერთო კლასში. სასაზღვრო ალიფატური ალდეჰიდების და კეტონების უდიდესი სიგანის ჰომოლოგიური სერიის ზოგადი ფორმულა იგივეა: Z n H 2p.
1. ნომენკლატურა
ა) ალდეჰიდების ტრივიალური სახელები უფრო ფართოა, სუნი ასოცირდება იგივე ნახშირბადის ჩონჩხის მქონე მჟავების ტრივიალურ სახელებთან, დაჟანგვისას ადვილად გარდაიქმნება ალდეჰიდებად: ფორმული ალდეჰიდი (ფორმალდეჰიდი), აცეტალდეჰიდი (აცეტალდეჰიდი), პროპიონი.
IUPAC ნომენკლატურის მიხედვით, ალდეჰიდის ჯგუფის არსებობა მითითებულია სუფიქსით. -al(-al):

ვინაიდან ალდეჰიდის ჯგუფი არ შედის სათავეებში ძველი ჯგუფების არსებობის გამო, იგი მითითებულია პრეფიქსით. ფორმები:

ბ) მარტივი კეტონების სახელები ემატება რადიკალების სახელებს, რომლებიც დაკავშირებულია კარბონილის ჯგუფთან, ეს სიტყვები კეტონი:

დასაკეცი კეტონების ვიკორისტის სახელებისთვის გამოიყენეთ სუფიქსი -გაიმარჯვე(IUPAC):

ხანდაზმული ჯგუფის არსებობისთვის, კეტონური ჯგუფი მითითებულია პრეფიქსით ოქსო -:

2. ფიზიკური ძალა
მოლეკულაში, იქნება ეს ალდეჰიდი თუ კეტონი, მჟავის ატომის უფრო დიდი ელექტროუარყოფითობის ბმული ტოლია ნახშირბადის ატომს, დაშლილი ელექტრონები და >C=0 ჯგუფში π-ბმული დაკავშირებულია მჟავას ატომთან. . ამის მიზეზია ნახშირბადის ატომებზე (δ-) ზედმეტი ელექტრონული უფსკრულის გამოჩენა და ნახშირბადის კარბონილის ატომზე (δ+) ელექტრონული უფსკრულის მნიშვნელოვანი ცვლილება, რაც იწვევს σ-ელექტრონული ნახშირბადის ნახშირბადში გადაადგილებას. ატომები:

ამ თანმიმდევრობით, ალდეჰიდები და კეტონები არის პოლარული მეტყველება მჟავას ატომზე მსოფლიო ელექტრონული ფარით. ოქსო ნაერთების პრაქტიკულად ყველა ქიმიური რეაქცია დაკავშირებულია მოლეკულაში ელექტრონის სიმკვრივის ასეთი განაწილებით.
ქვედა ბმული С=0 є ერთი საათი და მეტი რეაქციული და მეტი მიცნოი, ქვედა ბმული С=С. ასე რომ, C=O ბმის ენერგია 750 კჯ/მოლზე მეტია, რაც გაცილებით მეტია, C-O ბმის ქვედა ენერგია არის 360 2 = 720 კჯ/მოლი. რიგი zv'yazkiv Z=Z і Z-Z zvorotne spіvvіdnoshennia. C=C ბმის ენერგია (612 კჯ/მოლი) ოდნავ ნაკლებია, C-C ბმის ქვედა ენერგია უფრო დაბალია (339 2 = 678 კჯ/მოლი). C=O ბმის გაზრდილი რეაქცია C=Z პოლარობაში განსხვავდება Pro და C ატომების ელექტრონეგატიურობაში.
ალდეჰიდების და კეტონების მოლეკულების ნამსხვრევები სპირტებზე და ბევრი არამდგრადი ატომები წყალში, მათი მოლეკულები არ არის დაკავშირებული და მათი დუღილის წერტილი საგრძნობლად დაბალია, დაბალია ალკოჰოლებში. ზაგალომი არის ტროჰი ვიშის კეტონების დუღილის წერტილი, ალდეჰიდების ქვედა იზომერული. Razgaluzhennya lansyuga viklikaє დუღილის ტემპერატურის რეგულარული შემცირება. ქვედა წევრები დაბალია - აცეტონი, ფორმალდეჰიდი, აცეტალდეჰიდი - საცალო ვაჭრობა სასმელ წყალში, სხვა ალდეჰიდები და კეტონები უფრო მნიშვნელოვანია, ვიდრე უმსხვილესი ორგანული საცალო ვაჭრობა (ალკოჰოლი, ეთერი თხელი.). ქვედა ალდეჰიდებს აქვთ მკვეთრი სუნი, ალდეჰიდებს 3 -3 6 აქვთ მიუღებელი სუნი, უფრო მაღალ ალდეჰიდებს აქვთ ყვავილოვანი სუნი და პარფიუმერიაში ჩერდებიან.
ალდეჰიდები და მათი ქიმიური ძალა
ალდეჰიდები ისეთი ორგანული მეტყველებაა, რომელთა მოლეკულებში კარბონილის ჯგუფი შეკრულია, სულ მცირე, წყლის ერთ ატომთან და ნახშირწყლების რადიკალთან.
ალდეჰიდების ქიმიური ძალა განისაზღვრება მოლეკულაში კარბონილის ჯგუფის არსებობით. კარბონილის ჯგუფის მოლეკულაზე ციმთან კავშირი შეიძლება იყოს შემთხვევითი რეაქციის მანიშნებელი.
მაგალითად, თუ თქვენ იღებთ და გამოტოვებთ ფსონ ფორმალდეჰიდს ნიკელის კატალიზატორის წყალთან ერთად, მაშინ წყლისა და ფორმალდეჰიდის დამატება გადაიქცევა მეთილის სპირტად. Krіm tsgogo, tsy zv'yazku ქვირითის პოლარული ხასიათი და ალდეჰიდების ისეთი რეაქცია, როგორიცაა წყლის გამოჩენა.
ახლა კი გადავხედოთ რეაქციების ყველა მახასიათებელს წყლის სახით. შემდეგი ნაბიჯი არის კარბონილის ჯგუფის კარბონილის ატომში ჰიდროქსილის ჯგუფის დამატება, რომელიც ატარებს ნაწილობრივ დადებით მუხტს, მჟავას ატომის ელექტრონის ორთქლს.

ასეთი შემთხვევითი დამახასიათებელი შეურაცხმყოფელი რეაქციით:
პირველ რიგში, ჰიდროგენიზაცია ხორციელდება და პირველადი სპირტი RCH2OH იხსნება.
სხვაგვარად საჭიროა სპირტების დამატება და სპირტების R-CH (OH) - OR დაშლა. ხოლო ჰიდროქლორინის HCl-ის არსებობისას, რომელიც მოქმედებს როგორც კატალიზატორი და ჭარბი ალკოჰოლით, გვეშინია აცეტალი RCH (OR) 2;
მესამე, აუცილებელია ნატრიუმის ჰიდროსულფიტში NaHSO3-ის დამატება და მსგავსი ჰიდროსულფიტ ალდეჰიდების დაშლა. ალდეჰიდების დაჟანგვამ შეიძლება გამოიწვიოს ისეთი განსაკუთრებული რეაქციები, როგორიცაა ურთიერთქმედება ამონიუმის ოქსიდის შრიბლ (I) და midi (II) ჰიდროქსიდთან და კარბოქსილის მჟავების ელიმინაცია.
ალდეჰიდების პოლიმერიზაციის დროს დამახასიათებელია ისეთი განსაკუთრებული რეაქციები, როგორიცაა წრფივი და ციკლური პოლიმერიზაცია.
როგორ ვისაუბროთ ალდეჰიდების ქიმიურ ძალაზე, შემდეგ გამოიცნოთ ჟანგვის რეაქცია. ასეთ რეაქციებამდე შეიძლება დავამატოთ ვერცხლის ძერკალას რეაქცია და სვეტლოფორის რეაქცია.
ციმბირის ძერკალას უჩვეულო რეაქციას შეგიძლიათ კლასში ციკავიუს დოსვიდით შემოწმებით უყუროთ. რისთვისაც გჭირდებათ სუფთა ვიმიტის სინჯარა, ჩაასხით ჭიქაში მცირე რაოდენობით ამონიუმის ოქსიდი და შემდეგ დაამატეთ ცოტაოდენი ჩოტირი ან ფორმალინის ხუთი წვეთი. შემდეგ ეტაპზე, ტესტის ჩატარებისას, აუცილებელია სინჯარის მოთავსება კოლბაში ცხელ წყალში და ამავდროულად შეძლებთ გამოიყურებოდეს როგორც ცქრიალა ბურთი გამოდის ტესტის კედლებზე. მილის. Tse pokrittya є ალყაში ლითონის srіbl.

და ღერძს ეწოდება "სვეტლოფორის" რეაქცია:

ალდეჰიდების ფიზიკური ძალა
ახლა მოდით შევხედოთ ალდეჰიდების ფიზიკურ ძალებს. როგორ შეუძლიათ ძალებს, რომლებსაც შეუძლიათ ლაპარაკი? ყურადღება მიაქციეთ მათ, რომ რიგი მარტივი ალდეჰიდები არის უნაყოფო აირი, დაკეცილი წარმოდგენები სამშობლოს თვალწინ და მთავარი ალდეჰიდების ღერძი არის მეტყველების სიმტკიცე. რაც უფრო დიდია ალდეჰიდების მოლეკულური წონა, მით მეტია დუღილის წერტილი. მაგალითად, პროპიონის ალდეჰიდი დუღილს აღწევს 488 გრადუსზე, ხოლო პროპილ სპირტის ღერძი დუღს 978 0C-ზე.
თუ საუბრობთ ალდეჰიდების სიმრავლეზე, მაშინ ეს ერთისთვის ნაკლებია. ასე, მაგალითად, ოსტოვი და მურაშინი ალდეჰიდები შეიძლება უძლური იყოს წყლის მიხედვით ცვალებადობაზე, ხოლო დაკეცილი ალდეჰიდები შეიძლება დაასუსტონ შენობის როზჩინენიამდე.
ალდეჰიდებს, რომელთა დანახვა ყველაზე დაბალ დონეზეა, მკვეთრი და მიუღებელი სუნი აქვთ, ხოლო წყალში გაურკვეველი მყარი ნივთიერებები კი სასიამოვნო ყვავილოვანი სუნით ხასიათდება.
ბუნებაში ალდეჰიდების ცოდნა
ბუნებაში, ალდეჰიდების სხვადასხვა ჯგუფის წარმომადგენლები ყველგან ჩნდებიან. სუნი არის როსლინების მწვანე ნაწილებში. ეს არის ალდეჰიდების ერთ-ერთი უმარტივესი ჯგუფი, რომელშიც გვხვდება ფორმალური ალდეჰიდი CH2O.
ალდეჰიდები ასევე მუშავდება დაკეცილი საწყობით. ასეთი ხედების წინ დევს ვანილინი და ყურძნის ცუკორი.
თუმცა, ვინაიდან ალდეჰიდები ადვილად შედიან ყველა სახის ურთიერთქმედებაში, მათ შეუძლიათ დაექვემდებარონ დაჟანგვას და განახლებას, მაშინ შეგვიძლია დარწმუნებით ვთქვათ, რომ ალდეჰიდები ჩვეულებრივზე მეტია იშვიათი რეაქციების მიმართ და რომ სუფთა გარეგნობისას სუნი უფრო გამოხატულია. და მათი პოხიდნის ღერძი ყველგან ჩანს, როგორც მზარდი შუაში, ასევე არსებები.

ალდეჰიდების სტაზი
ალდეჰიდნა ჯგუფი წარმოდგენილია ბევრ დაბალ ბუნებრივ გამოსვლებში. Їx დამახასიათებელი ბრინჯი, აიღეთ ბაგატები მათგან, є სუნი. ასე, მაგალითად, უმაღლესი ალდეჰიდების წარმომადგენლები ივსებიან სხვადასხვა არომატით და შედიან ეთერული ზეთების საწყობში. ისე, როგორც უკვე იცით, ასეთი ოლიები გვხვდება ყვავილოვან, ცხარე და ცხარე ვარდებში, ხილსა და ხილში. სუნებმა იცოდნენ ხელსაქმის შერჩევის მასშტაბები და სუნამოების შერჩევა.
ალიფატური ალდეჰიდი CH3(CH2)7C(H)=Pro გვხვდება ციტრუსის ეთერზეთებში. ასე რომ, ალდეჰიდებს ფორთოხლის სუნი აქვთ და ჩერდებიან კვების მრეწველობაში, როგორც არომატიზატორი, ასევე კოსმეტიკაში, პარფიუმერიაში და ბუტოვის ქიმიაში, როგორც სუნამო.
მურაშინი ალდეჰიდი არის არალულის გაზი, რომელსაც შეიძლება ჰქონდეს მკვეთრი სპეციფიკური სუნი, რომელიც ადვილად იშლება წყალში. ფორმალდეჰიდის ასეთ წყალხსნარს ფორმალინსაც უწოდებენ. ფორმალდეჰიდი უფრო ტოქსიკურია, მაგრამ მედიცინაში ის ჩერდება მოზრდილებში, როგორც სადეზინფექციო საშუალება ზასიბს. Yogo vikoristovuyut ხელსაწყოების დეზინფექციისთვის და yogo სუსტი rozchiny vikorivuyut ტყავის დასაბანად ძლიერი სასმელად.
გარდა ამისა, ფორმალდეჰიდი ენაცვლება გარუჯულ შკირს, რათა შენობა დაიფაროს თეთრი ენებით, როგორც საწყობში შკირში.
სასოფლო-სამეურნეო სახელმწიფოში ფორმალდეჰიდი სასწაულებრივად აღმოჩნდა მარცვლეულის მოსავლის ერთი საათით ადრე ბოლო რობოტებამდე. Yogo zastosovuyut წარმოების პლასტმასის, როგორც ეს ასე აუცილებელია ტექნიკა და buttock საჭიროებებს.
ოსტ ალდეჰიდი უნაყოფო სამშობლოა, რადგან მას აქვს ტკბილი ვაშლის სუნი და ადვილად იშლება წყალში. Zastosovuєtsya ღვინოები თვალის მჟავის მოსაცილებლად და სხვა გამოსვლებისთვის. ალე, ღვინის ნატეხები მყიფე მეტყველებით, მაშინ მას შეუძლია სხეულის განადგურების ვიბრაცია, ან თვალების ლორწოვანი გარსის ანთება და ველური გზები.
5.1. ზაგალნას მახასიათებელი
ალდეჰიდების და კეტონების საკამათო კლასებმა უნდა შეცვალონ ფუნქციური კარბონილის ჯგუფი და განიხილონ კარბონილის სპოლუკი.მათთვის სახელიც გამარჯვებულია ოქსოსპოლკი, oskіlki ჯგუფს \u003d O ეწოდება ოქსო ჯგუფს.
ალდეჰიდებს უწოდებენ ნახევრად გარსებს, რომლებშიც კარბონილის ჯგუფი ერთვის ორგანულ რადიკალს და წყლის ატომს; კეტონები - კარბონილის ნახევარი ორი ორგანული რადიკალით.
ჯგუფს -CH=O, რომელიც შედის ალდეჰიდების საწყობში, ე.წ ალდეჰიდი,ვიდპოვიდნო ჯგუფი კეტონებში - კეტონი,ან კეტოჯგუფი.
ორგანული რადიკალების ბუნების გამო ნაყოფს ალდეჰიდები და კეტონები შეიძლება მოჰყვეს ალიფატურიან არომატულირიგი; ketoni buvayut zmіshanimi(ცხრილი 5.1).

ალდეჰიდებსა და კეტონებს ყოველდღიური ურთიერთქმედება აქვთ მჟავე რუხლისა და წყლის ატომებთან ალკოჰოლის ზედაპირზე. ციმ ალდეჰიდებთან და კეტონებთან კავშირში ისინი არ არიან დაკავშირებული წყალში ხსნად ბმებთან, მაგრამ უფრო ნაკლებია, სანამ წყლის ბმები არ დაიშლება წყლის მოლეკულებთან და ამ სიკეთესთან ისინი გამოიყოფა მასში (განსაკუთრებით ჰომოლოგის პირველი წევრები სერია).
ცხრილი 5.1.ალდეჰიდები და კეტონები

5.2. ალდეჰიდების და კეტონების რეაქციის ცენტრები
sp 2 -კარბონილის ჯგუფის ნახშირბადის ატომის ჰიბრიდიზაცია ქმნის სამ σ-ბმას, რომლებიც დევს ერთ სიბრტყეში, და π-ბმა ატომთან მჟავე არაჰიბრიდირებული p-ორბიტალის რაჰუნოკისთვის. შედეგად, ნახშირბადის ატომების ელექტრონეგატიურობა და მათ შორის არსებული π-ბმათა მჟავიანობა ძლიერ პოლარიზებულია (ნახ. 5.1). შედეგად, კარბონილის ჯგუფის ნახშირბადის ატომებს აქვთ ნაწილობრივი დადებითი მუხტი δ+, ხოლო მჟავას ატომებს აქვთ ნაწილობრივი უარყოფითი მუხტი δ-. ნახშირბადის ოსკილკის ატომი ელექტრონის დეფიციტია, ღვინო არის ნუკლეოფილური შეტევის ცენტრი.
როზპოდილის ელექტრონული სიმძლავრე ალდეჰიდების და კეტონების მოლეკულებში ელექტრონული ინექციის გადაცემის გაუმჯობესებით

ბრინჯი. 5.1.ელექტრონული ბუდოვას კარბონილის ჯგუფი
კარბონილის ჯგუფის ნახშირბადის დეფიციტური ატომი σ-ბმულებიდან ნაჩვენებია სქემა 5.1-ში.
სქემა 5.1.რეაქციის ცენტრები ალდეჰიდების და კეტონების მოლეკულებში

ალდეჰიდების და კეტონების მოლეკულებს აქვთ რამდენიმე რეაქციის ცენტრი:
ელექტროლიტური ცენტრი - კარბონილის ჯგუფის ნახშირბადის ატომი - აღნიშნავს ნუკლეოფილური შეტევის შესაძლებლობას;
მთავარი ცენტრი - მჟავა ატომი - შესაძლებელს ხდის პროტონით შეტევას;
CH-მჟავის ცენტრი, წყლის ატომი, რომელსაც შეიძლება ჰქონდეს სუსტი პროტონის მსხვრევადობა და შესაძლოა, ზოკრემას, დაესხას ძლიერი ფუძე.
ზოგადად, ალდეჰიდები და კეტონები შეიძლება იყოს ძალიან რეაქტიული.
5.3. ნუკლეოფილური გაჩენა
ალდეჰიდებისა და კეტონებისთვის ყველაზე დამახასიათებელია ნუკლეოფილური დამატების რეაქციები. ა ნ.
ნუკლეოფილური ადსორბციის მექანიზმის სრული აღწერა ა ნ
ალდეჰიდის ან კეტონის კარბონილის ჯგუფის ნახშირბადის ატომზე ნუკლეოფილური შეტევის სიმარტივე განისაზღვრება ნაწილობრივი მნიშვნელობით.
დადებითი მუხტი ნახშირბადის ატომებზე, იოგოს გახსნილობა და საშუალო მჟავა-ტუტოვანი სიმძლავრეები.

ნახშირბადის კარბონილის ატომთან შეკრული ჯგუფების ელექტრონული ეფექტების აღმოფხვრის გამო, ნაწილობრივი დადებითი მუხტის δ+ მნიშვნელობა nth-ში ალდეჰიდებსა და კეტონებში იცვლება შემდეგ რიგში:

კარბონილის ნახშირბადის ატომის სივრცის ხელმისაწვდომობა იცვლება, როდესაც წყალი იცვლება უფრო დიდი ორგანული რადიკალებით, ამიტომ ალდეჰიდები უფრო რეაქტიულები არიან, ნაკლები კეტონები.

ნუკლეოფილური დამატების რეაქციების ზოგადი სქემა ა ნკარბონილის ჯგუფში შედის ნუკლეოფილური შეტევა ნახშირბადის კარბონილის ატომზე, რასაც მოჰყვება ელექტროტროფილის დამატება მჟავას ატომში.

მჟავე გარემოში კარბონილის ჯგუფის აქტივობა, როგორც წესი, იზრდება, ნამსხვრევები ნახშირბადის ატომზე მჟავა ატომის პროტონაციის შემდეგ იწვევს დადებით მუხტს. ვიკორალური ბგერების მჟავა კატალიზირება მხოლოდ იმ შემთხვევაში, თუ თავდამსხმელ ნუკლეოფილს აქვს დაბალი აქტივობა.
ინდუქციური მექანიზმის მიღმა ხდება ალდეჰიდების და კეტონების არაერთი მნიშვნელოვანი რეაქცია.
დიდი ძალა ალდეჰიდებში და კეტონურ რეაქციებში ხდება სხეულის გონებაში და რეაქციები წარმოდგენილია ცხვირსახოცის წინა ნაწილებში. ამ განყოფილებაში განხილული იქნება ალდეჰიდების და კეტონების ყველაზე მნიშვნელოვანი რეაქციები, როგორც ეს ნაჩვენებია სქემაში 5.2 ერთი შეხედვით.

ალკოჰოლის მიღება. ალკოჰოლი, ალდეჰიდებთან ურთიერთობისას, ადვილად იშლება ნაპივეცეტალი. Napіvacetals არ ჟღერს მათი შეუთავსებლობის გამო. როდესაც მჟავე გარემოში ძალიან ბევრი ალკოჰოლია, ნაპივეცეტალები გარდაიქმნება აცეტალები.

მჟავა კატალიზატორის სტაგნაცია აცეტალის აცეტალად გადაქცევის დროს ცხადი ხდება ქვემოთ გამოწვეული რეაქციის მექანიზმიდან. ახალ სესხში ცენტრალური ადგილი უკავია კარბოკატიონის (I) მიღებას, სტაბილიზირებულია ელექტრონის ატომის მჟავას გაუზიარებელი წყვილის ნაწილისთვის (+M-ეფექტი C2H5O ჯგუფის).

ნაპივეცეტალებისა და აცეტალების გარდაქმნის რეაქციები იყო მეტაბოლიტები, ამიტომ აცეტალები და ნაპივეცეტალიები ადვილად ჰიდროლიზდება მჟავე გარემოში წყლის ჭარბი რაოდენობით. გუბეში, ნაპივეცეტალის ღერო, რადგან ალკოქსიდიონი არის ყველაზე მნიშვნელოვანი ჯგუფი, ქვედა ჰიდროქსიდ-იონი.
აცეტალების ხსნარები ხშირად ვიკორისტია, როგორც ალდეჰიდის ჯგუფის ტიმჩასოვური ზაჰისტი.
მოდი მანქანით. მიიყვანეთ კარბონილის ჯგუფში - დატენიანება- საპირისპირო რეაქცია. წყალგანაწილებაში ალდეჰიდის ან კეტონის დატენიანების საფეხურები უნდა იყოს დეპონირებული სუბსტრატში.
დატენიანების პროდუქტი, როგორც წესი, არ ჩანს დამატებითი დისტილაციისთვის, ღვინის ნამსხვრევები დევს გარე კომპონენტებზე. ფორმალდეჰიდი წყლიან ჰიდრატაციაში უფრო დაბალია 99,9%-ით, აცეტალდეჰიდი დაახლოებით ნახევარია, აცეტონი პრაქტიკულად არ არის დატენიანებული.

ფორმალდეჰიდმა (მურაშინი ალდეჰიდი) შეიძლება გამოიწვიოს ცილების მონელება. Yogo 40% წყლის წოდებები, წოდებები ფორმალინი, zastosovuetsya მედიცინაში, როგორც სადეზინფექციო ზასიბი და ანატომიური პრეპარატების კონსერვანტი.
ტრიქლოროძმარ ალდეჰიდი (ქლორალი) სრულად დატენიანებულია. იატაკის ელექტრონის ამომყვანი ტრიქლორომეთილის ჯგუფი სტაბილიზებს ქლორაჰიდრატს, რაც კრისტალურ მეტყველებას წყალს აქცევს მხოლოდ დისტილაციის დროს დეჰიდრატირებული გამონათქვამების არსებობისას - გოგირდის მჟავა და სხვა.

CC1 ქლორაჰიდრატის ფარმაკოლოგიური ეფექტის საფუძველზე s CH (VIN) 2 მოათავსეთ სპეციფიური ინექცია ალდეჰიდის ჯგუფის სხეულზე, რომელიც ითვალისწინებს სადეზინფექციო ძალას. ჰალოგენის ატომები ხელს უწყობენ მეტყველების ტოქსიკურობის შემცირებას, ხოლო კარბონილის ჯგუფის დატენიანება ამცირებს მეტყველების ტოქსიკურობას წვის გზით.
ამინოების და მათი მკვდრების გამოჩენა. ამინოები და სხვა აზოტოვანი ნაერთები სათესლე ფორმულიდან NH 2 X (X = R, NHR) რეაგირებს ალდეჰიდებთან და კეტონებთან ორ ეტაპად. ნუკლეოფილური ნაზავის პროდუქტები იწელება ზურგზე, შემდეგ კი არასტაბილურობის გამო გამოყოფს წყალს. ამ პროცესთან დაკავშირებით ისინი მას რეაქციად აფასებენ. ჩამოსვლა-გათიშვა.

სხვადასხვა პირველადი ამინოებს აქვთ ჩანაცვლება სახელი(მათ ასევე ეძახიან შიფის ქვესადგურები).
იმენი - მდიდარი ფერმენტული პროცესების შუალედური პროდუქტები. Otrimannya iminiv უნდა გაიაროს ამინო ალკოჰოლის გარდაქმნის სტადია, თითქოს ისინი გახდებიან ეფექტური, მაგალითად, როდესაც ფორმალდეჰიდი ურთიერთქმედებს α-ამინომჟავებთან (დივ. 12.1.4).
Іmini є სამრეწველო პროდუქტების მიერ ამინების ფლობა ალდეჰიდებთან და კეტონებთან ერთად dnovlyuvalnogo amіnuvannya.ეს მგზნებარე მეთოდი ეფუძნება კარბონილის ნაერთის ამიაკის (ან ამინის) ჯამის ინოვაციას. პროცესი მიმდინარეობს იმინის დამტკიცებიდან advent-გაყოფის სქემის მიხედვით, რაც დადასტურებულია ამინში.
როდესაც ალდეჰიდები და კეტონები ურთიერთქმედებენ მსგავს ჰიდრაზინთან, ჰიდრაზონი.ეს რეაქცია შეიძლება იყოს გამარჯვებული ალდეჰიდების და კეტონების დანახვისთვის ჯამებით და ქრომატოგრაფიული იდენტიფიკაციით.

დასაბუთებული შიფი და სხვა მსგავსი ჯიშები ადვილად ჰიდროლიზდება მინერალური მჟავების წყლის ხარისხით, გარე პროდუქტების ფუძიდან.
ყველაზე ხშირად ალდეჰიდების და კეტონების აზოტოვანი ფუძეებთან რეაქციისთვის საჭიროა მჟავა კატალიზი, რაც დააჩქარებს პროდუქტის გაუწყლოებას. თუმცა, თუ ნიადაგის მჟავიანობას ძალიან ადრე გაზრდით, მაშინ რეაქცია მოხდება აზოტოვანი ფუძის არარეაქტიულ მჟავად XNH-ად გადაქცევის შედეგად. 3+.
პოლიმერიზაციის რეაქცია. ძალაუფლების რეაქცია უფრო მნიშვნელოვანია, ვიდრე ალდეჰიდები. მინერალური მჟავებისგან გაცხელებისას ალდეჰიდების პოლიმერები იშლება პროდუქტებში.
პოლიმერების ხსნარი შესაძლებელია მეორე მოლეკულაზე კარბონილალდეჰიდის ატომის ერთი მოლეკულის მჟავა ატომის მიერ ნუკლეოფილური შეტევის შედეგად. ასე რომ, როდესაც ფორმალინი დგას, ის იშლება პოლიმერ ფორმალდეჰიდის - პარაფორმის თეთრ ნალექში.
5.4. კონდენსაციის რეაქციები
CH-მჟავის ცენტრის არსებობა ალდეჰიდის ან კეტონის მოლეკულაში უნდა მიიტანოს იქამდე, რომ ამ კარბონილის ნახევრების წყლის α-ატომებმა შეიძლება გამოიწვიოს პროტონის მსხვრევადობა. ასეთი პროტონების პრინციპით, პროტონები შეიძლება დაემატოს დამტკიცებულ კარბანიონებს. კარბანიონები ასრულებენ ნუკლეოფილების როლს კარბონილის სუბსტრატთან მიმართებაში. მიზეზი არის რეაქციების შესაძლებლობა, რომლის დროსაც ერთი მოლეკულა, როგორც ნუკლეოფილი, უერთდება ნეიტრალური კარბონილის ერთეულის სხვა მოლეკულის კარბონილის ჯგუფს. ასეთი პროცესები შეიძლება შეინიშნოს კონდენსაციის რეაქციამდე.
კონდენსაციას ეწოდება რეაქცია, რომელიც იწვევს ნახშირბად-ნახშირბადის ნახშირის ახალი ბმის წარმოქმნას, უფრო მეტიც, ორი ან მეტი აშკარად მარტივი მოლეკულისთვის იქმნება ახალი, კოლაფსირებული მოლეკულა.
ასე რომ, გუბეში, აცეტალდეჰიდის ორი მოლეკულა იხსნება ჰიდროქსიალდეჰიდი ნახშირბადის ატომების ორმაგი რაოდენობით.
რეაქციის პროდუქტს, რომელიც ცვლის ჰიდროქსილისა და ალდეჰიდის ჯგუფებს, ე.წ ალდოლი(ხაზების ჩათვლით ალდ ეგიდირომ ალკოჰოლიოლ), და თავად რეაქცია დასახელდა ალდოლის კონდენსაცია,ან ალდოლის ადვენტი.
ალდოლის კონდენსაციის მექანიზმი. კარბონილის ადგილზე ფუძის გაყოფისას, α-პოზიციიდან პროტონი იყოფა და კარბანიონი (I) იხსნება, რომელშიც უარყოფითი მუხტი დელოკალიზებულია კარბონილის ჯგუფის მონაწილეობით.

ანიონი (I) არის ძლიერი ნუკლეოფილი (ფერების აღნიშვნის მექანიზმის მოწინავე ეტაპზე), რომელიც უერთდება სხვა (უნიონირებულ) კარბონილის მოლეკულას. ამ ურთიერთქმედების შედეგად წარმოიქმნება ახალი C-C ბმა და იხსნება შუალედური ალკოქსიდის იონი (II). წყლიან გარემოში ანიონი სტაბილიზდება, პროტონს ყოფს წყლის მოლეკულად და გარდაიქმნება ტერმინალურ პროდუქტად - ალდოლად.

ალდოლის დამატების რეაქცია ნაჩვენებია პროპანალის მაგალითზე (მოლეკულა ჩანს ფერად, რომელიც უერთდება სხვა მოლეკულის C=Pro ჯგუფს); მსგავსი რეაქცია გამოიწვია აცეტონის კონდახით.

კონდენსაციის პროდუქტი - ალდოლი - გროვდება წყლის გაყოფამდე α,β-უჯერი კარბონილის ნაერთის ხსნარებით. Zvuchay tse v_dbuvaєtsya for podvischenoї ტემპერატურა. და აქ რეაქციას ცეცხლი ჰქვია კროტონის კონდენსაცია.
კონდენსაციის რეაქციები შეიძლება განვითარდეს სხვადასხვა ვარიანტში, სხვადასხვა კარბონილის ნახევრით, უფრო მეტიც, ერთ-ერთმა მათგანმა შეიძლება შურისძიება არ მოახდინოს CH-მჟავას ცენტრზე, როგორიცაა, მაგალითად, ფორმალდეჰიდი და ბენზალდეჰიდი შეტევითი რეაქციების დროს:

ალდოლის კონდენსაცია - საპირისპირო რეაქცია; საპირისპირო პროცესი ეწოდება ალდოლნი ყოფს(ან რეტროალდოლის რეაქცია). შეტევითი რეაქციები ხდება ბევრ ბიოქიმიურ პროცესში.
5.5. გამაგრება და დაჟანგვა
ხელახალი გამოგონებაალდეჰიდები და კეტონები გამოიყენება დამატებითი რთული ლითონის ჰიდრიდებისთვის LiAlH 4 , NaBH 4 . რეაქცია მოიცავს კარბონილის ატომის ნუკლეოფილურ შეტევას ნახშირბადის ჰიდრიდ-იონთან.
ალკოჰოლის მცირე ჰიდროლიზით, დაბინძურების შემდეგ, გამოდის პირველი ან მეორე სპირტი.

დაჟანგვაკარბოქსილის მჟავებში ალდეჰიდებზე გავლენას ახდენს ჟანგვის აგენტების დიდი რაოდენობა, მათ შორის მჟავე. რბილ გონებაში კეტონები არ იჟანგება.

ოქსიდი srіbla ამინოკომპლექსის მსგავსად 2 OH (Tollens' reagent) აჟანგებს ალდეჰიდებს კარბოქსილის მჟავებში, ლითონის srіblo ჩანს თავისთავად. ჟღერს სახელი - რეაქცია "ციმბირის სარკე".
ასევე, ალდეჰიდები ადვილად იჟანგება midi(II) ჰიდროქსიდით გუბეში.
შეურაცხმყოფელი რეაქციები ხშირად ძლიერდება, თითქოს ალდეჰიდის ჯგუფის გამოვლინებაა, თუმცა სუნი არასპეციფიკურია ალდეჰიდებთან მიმართებაში: დაჟანგვა მნიშვნელოვანი რეაგენტებით, მაგალითად, მდიდარი ატომური ფენოლებით, ამინოფენოლებით, არომატული ამინებით, ჰიდროქსიდის კეტონებით და ადვილად იჟანგება.
1. ალდეჰიდები და კეტონები: ბუდოვა, იზომერია, ნომენკლატურა. ქიმიური ძალა. საბაზისო. ნუკლეოფილური ნაერთების რეაქციები. ალკოჰოლისა და ნახშირწყლების გადახედვა. არომატული ალდეჰიდების და კეტონების რეაქციები არომატული ბირთვის მონაწილეობისთვის.
ალდეჰიდები და კეტონები გვხვდება მდე კარბონილისორგანული კოლექციები.
კარბონილის ნახევარებს ორგანულ მეტყველებას უწოდებენ, რომელთა მოლეკულებში არის C=O ჯგუფი (კარბონილი ან ოქსოჯგუფი).
კარბონილის ყლორტების ზოგადი ფორმულა:
ფუნქციურ ჯგუფს -CH \u003d Pro ეწოდება ალდეჰიდი.
ქეტონი- ორგანული მეტყველება, რომლის მოლეკულები ცვლის კარბონილის ჯგუფს, მიღებული ორი ნახშირწყლების რადიკალისგან. გლობალური ფორმულები: R 2 C \u003d O, R - CO - R 'ან
ვარსკვლავი C=Pro ძლიერ პოლარულია. Її დიპოლური მომენტი (2.6-2.8D) საგრძნობლად მაღალია, დაბალი С–О კავშირში სპირტებში (0.70D). ელექტრონები, რომლებიც წარმოადგენენ C=O ბმის ნამრავლს, განსაკუთრებით ყველაზე დამანგრეველი p-ელექტრონები, გადაინაცვლებს მჟავიანობის ელექტროუარყოფით ატომში, რაც იწვევს ახალი ნაწილობრივი უარყოფითი მუხტის გამოჩენას. კარბონილის ნახშირბადი დამუხტულია ნაწილობრივი დადებითი მუხტით.
ამიტომ ნახშირს ესხმის ნუკლეოფილური რეაგენტები, ხოლო ჟანგბადის საწვავს - ელექტროქიმიური, მათ შორის H+.
ალდეჰიდების და კეტონების მოლეკულებს აქვთ ყოველდღიური ატომები და წყალი, რომლებიც გრძელდება წყლის ბმების დაშლამდე. ამიტომ ალკოჰოლური სასმელების დუღილის წერტილი უფრო დაბალია, უფრო დაბალი. მეთანალი (ფორმალდეჰიდი) - გაზი, ალდეჰიდები C 2 -C 5 და კეტონები C 3 -C 4 - rіdini, vischi - მძიმე მეტყველება. ქვედა ჰომოლოგები წყალში განსხვავებულია, წყალში ხსნადი ბმები იქმნება წყლის მოლეკულებს, წყლის მოლეკულებსა და ნახშირმჟავას ატომებს შორის. ნახშირწყლების რადიკალის მატებასთან ერთად წყლის მრავალფეროვნება მცირდება.
სისტემატური სახელები ალდეჰიდებიმე ვიქნები შემდეგ სახელი vodpovidny ნახშირწყლების და დამატებით სუფიქსი -ალ. ლანცეტის ნუმერაცია იწყება ნახშირბადის კარბონილის ატომიდან. ტრივიალური სახელები ვიბრირებს ამ მჟავების ტრივიალური სახელების სახით, რადგან ალდეჰიდები გარდაიქმნება დაჟანგვის დროს.
სისტემატური სახელები კეტონებიარათანმიმდევრულად ვიბრირება რადიკალების სახელით (გაზრდის თანმიმდევრობით) სიტყვის დამატებით კეტონი. Მაგალითად:
CH3-CO-CH3 - დიმეთილი კეტონი(აცეტონი);
CH 3 CH 2 CH 2 -CO-CH 3 - მეთილპროპილი კეტონი.
ველურ ტიპში კეტონის სახელს მოჰყვება ნახშირწყლების ტიპის სახელი და სუფიქსი. -გაიმარჯვე; ლანცეტის ნუმერაცია იწყება კარბონილის ჯგუფთან ყველაზე ახლოს მყოფი ლანცეტის რანგიდან (IUPAC შემცვლელი ნომენკლატურა).
მიმართვა:
CH 3 -CO-CH 3 - პროპანი ღვინო(აცეტონი);
CH 3 CH 2 CH 2 -CO-CH 3 - პენტანი ღვინო- 2;
CH 2 \u003d CH-CH 2 -CO-CH 3 - პენტენი-4 - ღვინო- 2.
ალდეჰიდების და კეტონების ნომენკლატურა.
ალდეჰიდები და კეტონები ხასიათდება სტრუქტურული იზომერიზმი.
იზომერიზმი ალდეჰიდები:
ინტერკლასობრივი იზომერიზმი (ალდეჰიდის მსგავსი).
ნუკლეოფილური ნაერთების რეაქციები.
ალდეჰიდები და კეტონები ადვილად დასამატებელია ნუკლეოფილური რეაგენტების C=Pro ბმული. პროცესი იწყება ნუკლეოფილის შეტევით კარბონილის ნახშირბადის ატომზე. ავიღოთ ტეტრაჰედრული შუალედური, რომელიც წყდება პირველ ეტაპზე, ამატებს პროტონს და იძლევა პროდუქტს:
კარბონილის ნაერთების აქტივობა Ad N-რეაქციებში (ნუკლეოფილური დანამატის რეაქციები) დამოკიდებულია კარბონილის ნახშირბადის ატომზე ეფექტური დადებითი მუხტის სიდიდეზე და შემცვლელების დამოკიდებულებაზე კარბონილის ჯგუფზე. ელექტროდონორი და მოცულობის შუამავლები ხელს უწყობენ რეაქციას, ელექტრონის მიმღები შუამავლები ხელს უწყობენ ნახშირბადის ქარხნის რეაქციის აგებას. ამიტომ, ალდეჰიდები ად N-რეაქციებში აქტიური, ქვედა კეტონებია.
ალკოჰოლებისა და თიოლების მიღება.
ალდეჰიდები ამატებენ ალკოჰოლს გადაწყვეტილებებში დალიეთ აცეტალები. ალკოჰოლის სიჭარბით და მჟავა კატალიზატორის თანდასწრებით, რეაქცია შორს წავიდა - სანამ აცეტალები
არ მისცეთ კეტალები მსგავსი გონებისთვის.
თიოლები, როგორც ძლიერი ნუკლეოფილები, ამცირებენ ალკოჰოლს, ხსნიან ალდეჰიდებთან და კეტონებთან შერევის პროდუქტებს.
ჰიდროციანმჟავას მიღება
ჰიდროციანური მჟავა იზრდება კარბონილის ნახევრად გახსნილი ციანგიდრინების ძირითადი კატალიზატორების გონებაში.
ნატრიუმის ბისულფიტის დამატება.
ალდეჰიდი და მეთილის კეტონიუმი ამატებენ ნატრიუმის ბისულფიტს NaHSO 3 ბისულფიტის ნაერთების ხსნარებს.
მოდი მანქანით.
ალდეჰიდები და კეტონები ამატებენ წყალს ჰიდრატების ხსნარებს. რეაქცია საპირისპიროდ მიმდინარეობს. ჰიდრატები, რომლებიც დნება, არ არის თერმოდინამიკურად სტაბილური. Rivnovagu შეიცვალა bik produktіv priednannya ნაკლებად სხვადასხვა აქტიური კარბონილის შლაკები.
აზოტოვანი ფუძეების ნუკლეოფილური დამატების რეაქციები.
სანამ ეს რეაქციები ტყუილია:
ა) იმინის (აზომეტინის) განმანათლებლობა - შიფის საფუძვლები
გ) ჰიდრაზონების მიღება
დ) ნახევრადკარბაზონების სინთეზი
ალკოჰოლისა და ნახშირწყლების გადახედვა.
წყლის დამატება ალდეჰიდის მოლეკულებში გვხვდება ქვედა რგოლის უკან კარბონილის ჯგუფში. ალდეჰიდების ჰიდროგენიზაციის პროდუქტი არის პირველადი ალკოჰოლი, კეტონები მეორადი.

ა) კლემენსენის შთაგონებით.
როგორც კარბონილის ნახევრად დასტა ორ მჟავებამდე, მაშინ ვიკორისტი ამ ტიპის განახლება
ბ) განახლება კიჟნერ-ვოლფის მიხედვით
ასეთი შთაგონება იმარჯვებს წყნარ ხეობებში, თუ შთაგონების ობიექტი სტაბილურია საძირკვლამდე.
ამიაკი ჟანგავს ფილის ჰიდროქსიდს OH, როდესაც მსუბუქად გახურდება ალდეჰიდებით (მაგრამ არა კეტონებით), აჟანგებს მას მჟავად და ხსნის თავისუფალ ლითონის ფილს. საცდელი მილივით, ერთგვარი რეაქციაში, ბულა ფრონტალურად მწირი იყო შუაში, წვრილი ბურთივით დაეცა შიდა ზედაპირზე - ვერცხლის სარკე დგებოდა:

კეტონები არ შედიან ასეთ რეაქციებში. მათ აქვთ "ჟორსტკე დაჟანგვა" - გახსენით ბმული C-C
ჰალოგენაციის რეაქცია. ალდეჰიდები და კეტონები ადვილად რეაგირებენ ჰალოგენებთან ა-ჰალოგენოვირუსების დასაშლელად:

არომატული ალდეჰიდების და კეტონების რეაქციები არომატული ბირთვის მონაწილეობისთვის.
არსებობს ასეთი ტიპის ნახშირბადის ნახევრად არენები.
ელექტროტროფიული ჩანაცვლების რეაქციაში არომატული ალდეჰიდები ნორმალურად შედიან ორიენტაციის წესების შესაბამისად. ალდეჰიდნა ჯგუფი - ელექტრონის ამომყვანი ჯგუფი, არ აჩვენებს -I; -M-ეფექტები და მიყვანილია მეტაორიენტაციამდე.
Მაგალითად:

აცეტოფენონის აზოტირება ადვილი დასაძლევია გამაღიზიანებელი ნარევით 0 0 С ტემპერატურაზე:
მ-ნიტროაცეტოფენონი
2. ნახშირწყლები. კლასიფიკაცია და ნომენკლატურა. ბუდოვი, კონფიგურაცია და კონფორმაცია.









ცოცხალ ბუნებაში ნახშირწყლებს შემდეგი ფუნქციები აქვთ:
- ენერგიის მიწოდება მეტაბოლურ პროცესებში (სახამებელი როსლინებში, გლიკოგენი ცოცხალ ორგანიზმებში);
- როსლინის კედლების სტრუქტურული კომპონენტები (ცელულოზა); - მოიპოვოს კონკრეტული ბიოქიმიური პროცესების სუბსტრატებისა და რეგულატორების როლი;
є ცხოვრების საწყობის ელემენტები მნიშვნელოვანი გამოსვლები: ნუკლეინის მჟავები, კოენზიმები, ვიტამინები და სხვა.
- ნახშირწყლები ემსახურება zhі ssavtsіv-ის ძირითად კომპონენტს და ადამიანები იზრუნებენ თანაბრად, ტანსაცმელზე და ცხოვრებაზე.
ნახშირწყლების მიღებამდე ემატება გრუბის დიეტის 60-70%. სუნი მნიშვნელოვანია მზარდი პროდუქტების დროს, რადგან პურის, მარცვლეულის, მაკარონის, საკონდიტრო ნაწარმის ძირითადი კომპონენტებია სიროვინი დუღილის მრეწველობაში, ჰარქიული მჟავების წარმოებაში: რვამჟავა, რძემჟავა, ლიმონი.
Tilki roslin zdatnі zdіysnyuvat povny სინთეზი ნახშირწყლებში ფოტოსინთეზის გზაზე, რომლის პროცესში წყალი და ნახშირორჟანგი გარდაიქმნება ნახშირწყლებად სონის სინათლის მოქმედებით, როგორიცაა dzherel ენერგია. ორგანიზმების არსებებს არ შეუძლიათ ნახშირწყლების სინთეზირება და მათი აღება მზარდი გერლიდან:
3. ბუდოვა, იზომერია, მონოფუძე კარბოქსილის მჟავების ნომენკლატურა. ქიმიური ძალა. რეაქციები ნუკლეოფილურ რეაგენტებთან. მჟავა ჰალოიდების შემცირება. ხელახალი გამოგონება. დეკარბოქსილირების რეაქციები. კარბოქსილის მჟავების ფუნქციური ეფექტები. დიკარბოქსილის მჟავები, ნომენკლატურა და ავტორიტეტი.

ზაგალნას ფორმულის საზღვარი ერთი. მანქანა. მჟავები 





![]()
კარბოქსილის მჟავები ფუნქციური მოგზაურობა, რომლებშიც ჩანს მჟავა ჰალოიდები, დაკეცილი ეთერები, ანჰიდრიდები, ამიდები და მჟავების ნიტრილები. ანჰიდრიდები, ამიდები და ნიტრილები შუა მჟავების გარეშე ყველაზე ხშირად შეუძლებელია ამოღება, ეს ხდება არაპირდაპირი მეთოდებით.



განახლება:
კარბოქსილის მჟავებს მხოლოდ უფრო ძლიერი გიდების დახმარება შეიძლება დაეყრდნოთ. ამიტომ, მჟავების დამატებით, ისინი არ შეიცავს ალდეჰიდებს, არამედ მხოლოდ პირველადი ალკოჰოლს.
შეგიძლიათ დიბორანი (BH3) 2 ვიკორატიოთ.
დეკარბოქსილაცია- CO2-ის გამოდევნა კარბოქსილის მჟავებიდან ან მათი მარილებიდან. დეკარბოქსილაცია ხორციელდება გათბობის გზით მჟავების ან ფუძეების თანდასწრებით. ამავდროულად ისმის წყლის ატომის კარბოქსილის ჯგუფის ჩანაცვლება.
შეუცვლელი მონოკარბოქსილის მჟავები დეკარბოქსილატდება მძიმე გონებაში.
დეკარბოქსილაცია უფრო ადვილია a-პოზიციაში ელექტრონის ამომყვანი შემცვლელების არსებობისთვის.
კარბოქსილის მჟავების კალციუმის და ბარიუმის მარილების გაცხელების (მშრალი დისტილაციის) საშუალებით დეკარბოქსილაცია - კეტონების მოცილების მეთოდი.
დიკარბოქსილის მჟავები. ნომენკლატურა და ძალაუფლება
4. ალკენი. ალკენების ელექტროტროფიული დამატების რეაქციები (რეაქცია Aდე): მარკოვნიკოვის წესი და განმარტება. ჰალოგენებისა და ბრომის წყლის თავისუფალი რადიკალების მიღება. ალილენის ჰალოგენაცია. ჰომოგენური და ჰეტეროგენული ჰიდროგენიზაცია.
ალკენები (ოლეფინები).ნახშირწყლებში, რომლებიც შურისძიებას იღებენ ნახშირ-ნახშირბადოვანი რგოლების ერთ ქვედანაყოფზე, ერთი შუბის შემთხვევაში მათ ალკენებს უწოდებენ. ზაგალნა რომ უხეში ფორმულა З n Н 2 n . სერიებს, რომელთა წევრები იყოფა (2H) n-ზე, იზოლიური რიგი ეწოდება. CH 2 \u003d CH 2-ის პირველი წარმომადგენელი (ეთენი - ეთილენი), sp 2 - ჰიბრიდიზაცია.
Ad E რეაქციები არის ალკენის ტრანსფორმაციის ძირითადი ტიპი. ჰალოგენებს, წყალბადის ჰალოგენებს, გოგირდის მჟავას, წყალს და სხვა ელექტროქიმიურ რეაგენტებს შეუძლიათ ალკენების ელექტროქიმიური მექანიზმის მიბაძვა.
რეაქციის ძირითადი მექანიზმი მოიცავს დაბალ ბოლო სტადიას:
პირველ ეტაპზე ელექტროტროფილი აყალიბებს p-კომპლექსს ალკენთან, რომელშიც დამოკიდებული ბმა მოქმედებს როგორც დონორი, ხოლო ელექტროტროფილი მოქმედებს როგორც ელექტრონის მიმღები. გარდა ამისა, p-კომპლექსი რეგულარულად გადანაწილდება კარბოკატიონში (s-კომპლექსი). ბოლო ეტაპზე შეინიშნება კარბოკატიონის ურთიერთქმედება ნუკლეოფილთან (Y -) დამტკიცებულ პროდუქტთან.
ალკენები რეაგირებენ ბრომთან და ქლორთან პროდუქტების დასაშლელად და ამატებენ ერთი მოლეკულის დამოკიდებულ კავშირს ჰალოგენთან, რომლის გამოსავლიანობა მჟავასთან ახლოსაა. ფტორი ასევე აქტიურია და იწვევს ალკენების განადგურებას. იოდის მოხვედრა ალკენებში უმეტეს შემთხვევაში შებრუნებულია საპირისპირო რეაქციით, რომელიც მსგავსია სხვა რეაგენტების მიმართ.
რეაქციებში, რომლებიც მოიცავს HX ტიპის პოლარული მოლეკულების დამატებით არასიმეტრიულ ალკენებს, წყალი ემატება ჰიდროგენიზებულ ნახშირბადის ატომს ჯაჭვის ბმულით (ანუ ნახშირბადის ატომი, რომელიც დაკავშირებულია წყალში ატომების უდიდეს რაოდენობასთან).
მარკოვნიკოვის წესების წინააღმდეგ მარხვაენიჭება vipadkah-ს, თუ შუამავალი უკაბელო კავშირისთვის დატენილია ღვინოების ელექტრონული სიმძლავრით, მაშინ. აჩვენებს ელექტრონის მიმღების ძალას (- მერომ/ან - მ-ეფექტი).
მაგალითად, ტრიქლოროპროპენის Cl 3 C-CH=CH 2 HX-თან რეაქციაში წყალი ადის ნაკლებად წყალბადირებულ ნახშირბადის ატომამდე, ხოლო X უფრო ჰიდროგენიზებულ ატომამდე. ეს განპირობებულია იმით, რომ СCl 3 ჯგუფი ავლენს უარყოფით ინდუქციურ ეფექტს და С=З ბმის p-ელექტრონული ბმა გადადის უფრო პატარა წყალბადირებულ ნახშირბადის ატომზე.
გარდა ამისა, თუ რეაქცია მოდის არა ელექტროქიმიურ, არამედ რადიკალურ მექანიზმზე, მაშინ მარკოვნიკოვის წესი ასევე არ გამოიყენება. ამრიგად, HBr-ის რეაქცია პროპილენთან პეროქსიდების (H 2 O 2 ან R 2 O 2 ) თანდასწრებით, რომლებიც ქმნიან თავისუფალ რადიკალურ ნაწილებს (HO ან RO), მიჰყვება რადიკალურ მექანიზმს და ეწინააღმდეგება მარკოვნიკოვის წესებს.
ალილის ჩანაცვლება ჰალოგენებით.
CH 2 \u003d CH-CH 3 + Cl 2 ® CH 2 \u003d CH-CH 2 Cl + HCl
კავშირის ასეთი პირდაპირი ქლორირება ალილის რადიკალის სტაბილურობის გამო, რომელიც მიიღება რადიკალ-ლანცეგის პროცესის განხორციელებისას:
ინიცირება:
Cl 2 + M ® 2Cl + M
ალკენების ჰომოგენური და ჰეტეროგენული ჰიდროგენიზაცია.
ალკენების ჰეტეროგენული და ერთგვაროვანი კატალიზური ჰიდროგენიზაციის ხაზი. ჰეტეროგენული ჰიდროგენიზაციის დროს გვხვდება წვრილად ფორმის ლითონის კატალიზატორები - პლატინი, პალადიუმი, რუთენიუმი, როდიუმი, ოსმიუმი და ნიკელი, ან სუფთა სახით, ან დეპონირებულია ინერტულ ცხვირზე - BaSO 4 CaCO 3 გააქტიურებული ნახშირბადი, Al 2 O 3 და ა.შ. ორგანული საშუალებები და მოქმედებს როგორც ჰეტეროგენული კატალიზატორები. მათ შორის ყველაზე აქტიურია რუთენიუმი და როდიუმი, ხოლო ყველაზე ფართოდ გამოიყენება პლატინი და ნიკელი. პლატინის ჟღერს შავი დიოქსიდი PtO 2 ფართოდ ცნობილია სახელწოდებით "ადამსის კატალიზატორი". პლატინის ჯგუფის ვიკორისტის სხვა აქტიური ლითონები ინერტულ ცვეთაზე, მაგალითად, Pd/C ან Pd/BaSO 4, Ru/Al 2 O 3; Rh/C და ში. ნახშირზე გამოყენებული პალადიუმი აკატალიზებს ალკენების ჰიდროგენიზაციას ალკანებად ალკოჰოლში 0-20 0 C ტემპერატურაზე და ნორმალურ წნევაზე. ნიკელი იმარჯვებს ეგრეთ წოდებული "რეინის ნიკელის" დანახვაზე.
ალკენებში ჩამოკიდებული რგოლი ჰიდროგენირებულია ჰიდროგენიზაციის უფრო დიდი ხარისხით სხვა ფუნქციურ ჯგუფებთან (C=O, COOR, CN და ა.შ.) გონებით (0-20 0 C და ატმოსფერული წნევით).
ლითონის კატალიზატორების ზედაპირზე ჰეტეროგენული ჰიდროგენიზაცია შეიძლება შეიცავდეს უამრავ მცირე ფრაქციებს, როგორიცაა ალკენების იზომერიზაცია და ნახშირბად-ნახშირბადის ცალკეული ბმების გაყოფა (ჰიდროგენოლიზი). ჰომოგენური ჰიდროგენაცია თავისუფლდება ამ nedolіkіv. უმოკლეს ჰომოგენური ჰიდროგენიზაციის კატალიზატორებია როდიუმის (I) ქლორიდის და რუთენიუმის (III) ქლორიდის კომპლექსები ტრიფენილფოსფინთან - ტრის(ტრიფენილფოსფინი) როდიუმის ქლორიდთან (Ph 3 P) 3 RhCl (ვილკინსონის კატალიზატორი) და ტრიფოჰენრიუმის (3H3Ph) ტრიპინთან ერთად. ).
ჰომოგენური კატალიზატორების მნიშვნელობა გავლენას ახდენს ქვებმულების მონო- ან ორივე ჩანაცვლების შერჩევითი ჩანაცვლების შესაძლებლობაზე ქვებმულების სამი და ტეტრა-ჩანაცვლების არსებობისას ორმაგი ბმების არსებობის დიდი განსხვავებების გამო.
5. ალკინი. ალკინების რეაქციები. CH-მჟავიანობა. აცეტილენი, ბუდოვა რომ ბატონობა. ელექტროტროფიული და ნუკლეოფილური რეაქციების რეაქციები, მათი მექანიზმები. ალკინების დაჟანგვა, ხელახალი განვითარება, ჰიდროგენიზაცია.
ალკინები (აცეტილენები).ნახშირწყლებში, რომლებიც შურისძიებას ახდენენ ნახშირბად-ნახშირბადოვანი კავშირის ერთ დაკარგვაზე, ლანცეოლატების შემთხვევაში მათ ალკინებს ან აცეტილენებს უწოდებენ. ზაჰალნა არის მთლიანი ფორმულა З n Н 2 n -2 . CHºCH (ეთინი - აცეტილენის) პირველი წარმომადგენელი.
ალკენების მსგავსად, ალკინები ნაკლებად აქტიურია ელექტროტროფიული დამატების რეაქციებში და უფრო აქტიურია ნუკლეოფილებთან რეაქციებში, მაგალითად, ამინებთან და ალკოჰოლატებთან. ტიმი არ არის ნაკლები, ალკინი, იაკი და ალკენები, უფრო ადვილია რეაგირება ელექტროქიმიურ რეაგენტებთან, ქვედა - ნუკლეოფილებთან. დიდად ჩქარობს მიიღოს spivvіdnoshnja shvidkosty რეაქცია alkenіv და alkіnіv nadaє ბუნება rozchinnіv.
sp-ჰიბრიდიზაციის ფოლადში ნახშირბადის ატომს შეიძლება ჰქონდეს უდიდესი ელექტრული ორიენტაცია, ასე რომ შეიძლება გამოიწვიოს ძლიერი C-H მჟავიანობააცეტილენის ტერმინალური ჯგუფები. წყლის ატომს, რომელიც გვხვდება ნახშირბადოვანი წამლის ბმის არსებობისას, უფრო დიდი მჟავიანობა აქვს, წყლის ქვედა ატომი არის ალკენები და ალკანები. ეს აიხსნება იმით, რომ C ატომები უფრო ძლიერად იზიდავს ელექტრონებს, ამიტომ პოლარიზაციის C-H ბმა და ელექტროდადებითი ატომები და წყალი მათში დიდ მჟავიანობას ავლენენ. აცეტილენისა და ა-ალკინიუმის მჟავიანობა ვლინდება შემდეგ რეაქციებში:
![]()
ამიდ-ანიონს აქვს მაღალი ბაზისურობა, რაც შესაძლებელს ხდის აცეტილენიდს იყოს უფრო სტაბილური. Vodnochas წყალი, volodyuschye მჟავიანობა pored აცეტილენით, დანარჩენი აცეტილენიდები: 
ნატრიუმი, კალიუმი და სხვა აცეტილენიდები გუბე ლითონებისა და ნამდვილი მარილებისგან, რომლებიც წარმოიქმნება ლითონის კატიონებისა და აცეტილენიდის ანიონებისგან. აცეტილენის მარილები მნიშვნელოვანი ლითონებით (Ag, Cu, Hg) - უპირველეს ყოვლისა ვარდის მარილები. Tse covalently zbudovani z'ednannya, გაურკვეველია წყალთან ახლოს. სუნი წყდება წყლის ხაზიდან.
1. დატენიანება. თავად კატალიზატორების დუმილის თანდასწრებით წყალი ტრიალებს სამჯერ, რაც მეტრომდეა:
2. ჰალოგენაცია. ქლორის, ბრომისა და იოდის დაშვება ალკინივში ელექტროქიმიური მექანიზმით, ასევე ნაკლები სითხის, დაბალი ალკენივის მიმართ. ტრანს-დიჰალოალკენები, რომლებიც იხსნება ციომასთან, ადვილად ჩანს, ნამსხვრევები უფრო შორს არიან ჰალოგენისგან (ქრომის ქლორი) და განიცდიან დიდ სირთულეებს:

3. ჰიდროჰალოგენაცია. ჰალოგენური წყლები ემატება ალკინებს ელექტროქიმიური მექანიზმით. მაგალითად, როდესაც წყალბადის ქლორიდი ემატება აცეტილენს, ქლოროვინილი და 1,1-დიქლოროეთანი თანმიმდევრულად გამოდის. ჰალოგენებისა და ჰალოგენების ალკინებში მოხვედრა შეიძლება მოხდეს რადიკალური მექანიზმით. ელექტროსტატიკური მიდგომისას გამოიყენება მარკოვნიკოვის წესი, რადიკალური მექანიზმის შემთხვევაში კი პირდაპირი მიდგომა.
4. დატენიანება. წყალი ემატება ვერცხლისწყლის სულფატის თანდასწრებით (კუჩეროვის რეაქცია), ან ჰეტეროგენულ კატალიზატორებზე, რომლებითაც აცეტილენი გამოდის ალდეჰიდი და სხვა აცეტილენის ნახშირწყლები - კეტონები ენოლების გადაჯგუფების გამო, რომლებიც იხსნება:

5. ალკოჰოლური სასმელების მიღება. ალკოჰოლური სასმელების გამოჩენა ალკოჰოლების თანდასწრებით არის ნუკლეოფილიის გაჩენის რეაქცია. შედეგად, ვინილის ეთერები და აცეტალები იხსნება:
6. HCN-ის მიღება. ციანოჰიდრინის მჟავა აცეტილენს უერთდება midi(I) მარილების თანდასწრებით, რის შედეგადაც იხსნება აკრილის მჟავა ნიტრილი (აკრილონიტრილი):
7. დაჟანგვა.


ალკინები იჟანგება კალიუმის პერმანგანატის მიერ ნეიტრალურ გარემოში ტომობრივი კავშირის გასწვრივ, ხსნის კარბოქსილის მჟავებს (კალიუმის მარილები იხსნება რეაქციის ტვინში):
შარდში აცეტილენი იჟანგება ოქსილის მჟავას კალიუმის მარილში - კალიუმის ოქსალატში.
8. აცეტილენიდების განათლება. ამავდროულად, წყლის ატომები იცვლება ლითონის ატომებით:
წინააღმდეგ შემთხვევაში, სხვადასხვა ლითონებისთვის:
9. წყლის ჩანაცვლება ჰალოგენებით. ჰიპოჰალოგენურობის შემთხვევაში, წყლის ატომები პოტრინის კავშირში შეიძლება შეიცვალოს ჰალოგენის ატომებით:
10. პოლიმერიზაცია. აცეტილენის რეაქციისა და ზასტოსოვური კალიზატორული პოლიმერიზაციის გონებაში ჩავარდნა შეიძლება სხვადასხვა გზით გაიაროს:
დიმერიზაციაიგი გამოიყენება წყალში ამონიუმის ქლორიდის და მიდი (I) ქლორიდის გასახსნელად, რომელშიც იხსნება ბუტინ-3-ენ-1 (ვინილაცეტილენი):
ტრიმერიზაციამიმდინარეობს 500-600 pro 3-ზე გააქტიურებული ნახშირბადის თანდასწრებით, რეაქციის პროდუქტია ბენზოლი (ზელინსკის რეაქცია):

ტეტრამერიზაციაიგი გამოიყენება რთული ნაერთების გავლენის ქვეშ ნიკელზე, ძირითადად იხსნება ციკლოოქტატეტრაენი-1,3,5,7:

10. მაგნიუმის ორგანული თაროების მიღება. მაგნიუმის აცეტილენიდის (იოციკის რეაგენტი) ნარევი, რომელიც გამარჯვებულია სხვადასხვა სინთეზისთვის, ამცირებს მეთილმაგნიუმის იოდიდის პროპორციას ალკინთან, რომელიც შეიცავს წყლის ატომს შებოჭვის დაკარგვით:
6. ჰალოგენირებული ნახშირწყლები. ნუკლეოფილური ჩანაცვლებისა და გაყოფის რეაქციები. არომატული ჰალოგენირებული.
ჰალოგენის მსგავსი ნახშირწყლები ჩანს ნახევარი, ასე რომ ერთი ან მეტი ატომის შეცვლა შესაძლებელია ჰალოგენის ატომებით.
ჰალოგენირებული ნახშირწყლები კლასიფიცირდება ნახშირწყლების რადიკალის ბუნების მიხედვით (ალიფატური, ალიციკლური და არომატული), ჰალოგენის ატომების რაოდენობა მოლეკულაში (მონო-, დი-, ტრი- და პოლიჰალოგენოვირუსი), ჰალოგენის ბუნების მიხედვით. (ფტორ-, ქლორო-, ბრომო-, იოდი). ), ნახშირბადის ატომის ბუნება, რომლითაც იგი აკავშირებს ატომს ჰალოგენთან (პირველადი, მეორადი და მესამეული ჰალოგენირებული).
ნომენკლატურა. IUPAC ნომენკლატურის მიხედვით, ჰალოგენირებული ნახშირწყლების სახელები ემატება მსგავსი ნახშირწყლების სახელებს. თავის უკანა მხარეს მიუთითეთ ჩანაცვლების პოზიცია რიცხვით (როგორც ეს აუცილებელია), შემდეგ დაასახელეთ ჰალოგენი (როგორც საჭიროა - მის წინ არის ატომების რაოდენობა) და დაამატეთ სახელი. მშობლის სტრუქტურა (ალიფატურ ჰალოგენისმაგვარ ჯაჭვებში, თავი ნახშირბადოვანი შუბი, ალიციკლურში და არომატულში - ციკლი).
ნუმერაცია იწყება ნახშირბადოვანი შუბის ჰალოგენის ბოლოდან ყველაზე ახლოს.

1 - ბრომოპროპანი 1,2 - ქლოროციკლოჰექსანი ქლორბენზოლი
ნუკლეოფილური ჩანაცვლების რეაქციები
არომატული ჰალოგენირებულიჰალოგენით ბირთვში (ჰალოგენარილი) - ინერტული მეტყველების ხაზის დასრულება ჰალოგენის გამომმუშავებელი ალიფატური რიგებით. ამიტომ, სუნი იძულებულია შევიდეს ნუკლეოფილური ჩანაცვლების რეაქციაში. ჰალოგენის ატომის ასეთი უმოქმედობა ჰალოგენარილებში აიხსნება იოგოს ნაწილობრივი გაორმაგებით ბენზოლის რგოლთან:

ცე გამოიცანი ჰალოგენის მსგავსი არანახშირწყლების ქცევა, რომელშიც ჰალოგენის ატომი გვხვდება ნახშირბადთან, რომელიც ასოცირდება ქვედა კავშირთან. ამიტომ, ნუკლეოფილურ რეაგენტებთან ჰალოგენარილების რეაქციების განსახორციელებლად, საჭიროა სწრაფი გონება (მაღალი ტემპერატურა და წნევა):

ჰალოგენების ატომები შეიძლება შეიცვალოს უსარგებლოებით და შეიძლება შეიცვალოს სხვადასხვა ნუკლეოფილებით, რომლებიც გამარჯვებულები არიან სხვადასხვა ბირთვების სინთეზისთვის:
ელიმინაციის (დაშლის) რეაქციები – დეჰიდროჰალოგენაცია
ელიმინაციის რეაქციის შედეგად ალკენიტი და წყალბადის ჰალოიდი იხსნება რამდენიმე ალკილის ჰალოიდში.
მაგალითად, როდესაც ეთილის ქლორიდი თბება მდელოზე, ალკოჰოლი შლის HCl-ს და ხსნის ეთილენს:
თუ იზრუნებთ, რომ ეს რეაქცია განახორციელოთ წყალში და არა ალკოჰოლში, მაშინ მთავარი პროდუქტი იქნება ალკოჰოლი და არა ალკენი.
რამდენიმე ასიმეტრიული ალკილჰალოგენური რეაქციების დროს დეჰიდროჰალოგენაცია ნორმალურად მიმდინარეობს ზაიცევის მმართველობა: წყლის ატომის გაყოფა HX-ის გაყოფის რეაქციებში წააგავს უმცირეს ჰიდროგენიზებულ ნახშირბადის ატომს.
7. არომატული ნახევარი (არენი). ბენზოლის არომატული ხასიათი. მიღწევის ენერგია, არომატულობის კრიტერიუმები. ბენზოლის ელექტროტროფიული ჩანაცვლების რეაქცია. ბუდოვის π- და σ- კომპლექსები. უშუალოდ ბენზოლის კილტებში შუამავლებში ჩასხმის შემდეგ, ელექტროტროფიული ჩანაცვლების რეაქციების სვიდკი.
არომატული ნახშირწყლების ძირითადი თვისება და π-ელექტრონული ნაერთის თანაბარი განაწილება მოლეკულაში. ერთი თარო არის π-ელექტრონების დახურული სისტემა ციკლურ მოლეკულაში - არომატულობის მთავარი ნიშანი. π-ელექტრონების ასეთი მემარჯვენეობისთვის აუცილებელი მენტალურია 2p-ორბიტალების ღერძების პარალელიზმი, რომლებიც მონაწილეობენ დახურული π-ელექტრონული სისტემის განათებაში. ამიტომ არომატული სპოლუკ ობოვიაზკოვოს მოლეკულები შრომობენ ბუდოვის თვითმფრინავს. მიუხედავად იმისა, რომ გონება არ არის დამარცხებული, π-ელექტრონების წრიული თანმიმდევრობა განადგურებულია. შედეგად, იატაკი არ არის არომატული. არომატულ ნახევრად გარსებს ასევე ახასიათებს π-ელექტრონების მცირე რაოდენობა მოლეკულაში. გერმანელი ქიმიკოსი-თეორეტიკოსი ე.ჰუკელი viviv p r და v l დაახლოებით (1931): ბრტყელი ციკლური ნახევარი, რომლის მიღებაც შესაძლებელია π-ელექტრონების სისტემისგან, შეიძლება იყოს არომატული, ამიტომ ამ ელექტრონების რაოდენობაა 4n + 2 (de p \u003d 0, 1, 2, 3 და ა.შ.). სხვა სიტყვებით რომ ვთქვათ, არომატულ ველებში შეიძლება ინახებოდეს 2, 6, 10, 14 ელექტრონი და ა.შ. იგივე წესი ვრცელდება მხოლოდ მონოციკლურ სპოლუკებზე.
მოლეკულები, როგორც დამახასიათებელი სტრუქტურული, ენერგეტიკული და ქიმიური ძალების ერთობლიობა, ჩახლართულია ბრტყელ ციკლურ სტრუქტურასთან კავშირების სისტემით, რომელიც ჩამოყალიბებულია დელოკალიზაციით.გვ-ელექტრონებს უწოდებენ არომატული იატაკები.
ერთადერთი მახასიათებელი, რომელიც საშუალებას გაძლევთ დაახარისხოთ იგი როგორც არომატული ან არა არომატული, არა არსებითი. არომატული სპოლუკების ძირითადი მახასიათებლებია:
skhilnіst ჩანაცვლების რეაქციებზე, მაგრამ არ მოდის (უბრალოდ უფრო ადვილია, ისტორიულად პირველი ნიშანი, კონდახი - ბენზოლი, vіdmіnu vіd ეთილენზე და არა znebarvlyuє ბრომის წყალში)
· ვიგრაში ენერგიაში, წყვილებში არაკონიუგირებული ქვებმულების სისტემით. მას ასევე უწოდებენ ენერგეტიკულ რეზონანსს (გაუმჯობესებული მეთოდი არის ენერგიის რეზონანსი დევარი) (დიდი იატაკი შესანიშნავია, რომ მოლეკულამ იცის მნიშვნელოვანი ტრანსფორმაცია, რათა მიაღწიოს არომატულ მდგომარეობას, მაგალითად, ციკლოჰექსადიენი ადვილად დეჰიდროგენდება ბენზოლად, ორი და ტრიატომური ფენოლები. მნიშვნელოვანია ფორმაში).
· რგოლის მაგნიტური სტრუმის გამოვლინება;
· თვით თვითმფრინავის არსებობა (მინიმალურად შექმნილი), რომელშიც დევს ყველა (მაგრამ არა ყველა - ჰომოარომულობა) ატომები, რომლებიც ქმნიან არომატულ სისტემას. პ-ელექტრონების იმავე რგოლში, რომლებიც ერთდროულად ყალიბდება კავშირების ქვეშ (ან ელექტრონები, რომლებიც შედიან ჰეტეროატომების რგოლში), დევს არომატული სისტემის სიბრტყის ზემოთ და ქვემოთ.
· პრაქტიკულად zavzhdim dotremuetsya Hückel-ის წესი: არომატული სისტემა ნაკლებად სავარაუდოა, რომ შურისძიება (at kіltsi) 4n + 2 ელექტრონი (de n = 0, 1, 2, ...). სისტემა, რომელიც შურისძიებას იღებს 4n ელექტრონების მიმართ, ანტიარომატიულია (უფრო მარტივი გაგებით, ეს ნიშნავს მოლეკულაში ზედმეტ ენერგიას, ობლიგაციების არათანაბარობას, დაბალ სტაბილურობას - რეაქციების მასშტაბურობას).
(ქლორბენზოლი) + H2O


Pokhіdnih ბენზოლი Z 6 N 5 Xშუამავლის ინფუზიის ქვეშ Xლ-ელექტრონული სიბნელის განაწილების თანასწორობა დარღვეულია, ტობტო. • პოპულარიზაციის სფეროები და შემცირებული ელექტრონული ძალა. ამიტომ ელექტროშეტევის სიმსუბუქე უშუალოდ შუამავლის ბუნებაშია.
ბენზოლის რგოლში დამცველებს შეუძლიათ მიიღონ ჩანაცვლებითი რეაქციები ( აქტიური ადვოკატები), და ასე გააუმჯობესეთ რეაქციის სიჩქარე ( შუამავლების გამორთვა).